肝脏的再生能力有多神奇?健康肝脏即便被切除三分之二,也能在几周内恢复原有大小。但在疾病、衰老等状态下,这份 “自愈超能力” 会大幅减弱,轻则术后恢复艰难,重则引发肝衰竭。长久以来,驱动肝脏再生的核心机制,一直是医学界亟待解开的谜题。

近日,发表于顶级期刊《自然・代谢》(Nature Metabolism)的一项重磅研究,终于找到了答案!美国宾夕法尼亚大学 Joseph A. Baur 教授领衔的团队证实,肝细胞线粒体中的烟酰胺腺嘌呤二核苷酸(NAD+)含量,正是调控肝脏再生速度的 “限速开关”。

这一发现首次明确了特定细胞器中特定分子的调控作用,为开发促进肝再生的精准疗法,点亮了全新方向。
PART 01
藏在细胞里的秘密:NAD + 的 “分区工作” 与专属运输管道
NAD + 素有 “长寿分子” 之称,是细胞能量代谢的核心辅因子,参与 DNA 修复、基因表达、能量合成等数百种生化反应,补充 NAD + 前体(NR、NMN)也被证实能改善代谢、延缓衰老。
但鲜为人知的是,NAD + 在细胞内并非均匀分布,而是分驻在细胞质、细胞核、线粒体等不同 “工作区”,不同区域的 NAD + 各司其职。其中,线粒体作为细胞的 “能量工厂”,其 NAD + 水平直接决定能量生产效率,而它的 NAD + 供应,也藏着一个关键秘密。
几年前 SLC25A51 基因的发现,成为研究的重要转折点:线粒体自身无法合成 NAD+,必须依靠 SLC25A51 这个 “专用运输管道”,从细胞质中主动摄取。这一发现,让精准调控线粒体 NAD + 水平成为可能,也为探索肝脏再生机制打开了突破口。
PART 02
基因剪刀下的真相:减少“管道”,再生即刻“减速”
为了验证线粒体NAD+是否对肝脏再生至关重要,研究团队利用基因工程技术,进行了一场大胆的实验。他们发现,完全缺失SLC25A51基因对小鼠是致命的,这足以证明该基因对生命的重要性。于是,他们转而创建了只携带一份功能基因的“杂合子”小鼠(Slc25a51+/-),这些小鼠外表看似与普通小鼠无异,但深入分析后,科学家们惊讶地发现,尽管它们肝脏组织的总NAD+水平没有变化,但线粒体内的NAD+含量却显著降低。这证实了SLC25A51确实是线粒体NAD+的“限速器”。
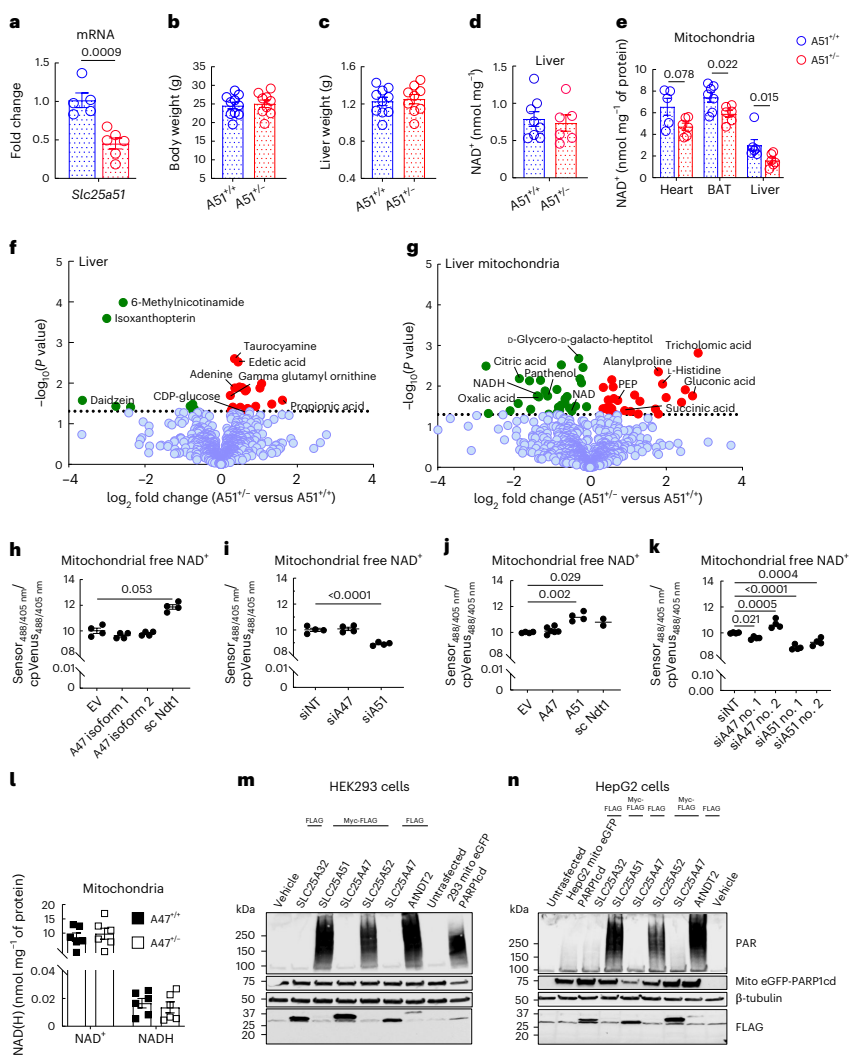
真正的考验在于肝脏再生实验。当这些小鼠经历三分之二肝脏切除后,与普通小鼠相比,它们的肝脏再生速度明显减缓,肝体重比恢复不佳,肝细胞分裂增殖的迹象也寥寥无几。这意味着,仅仅减少了线粒体这个“小房间”里的NAD+供应,就足以拖累整个肝脏的修复进程。线粒体NAD+的核心地位,在这一刻被清晰地揭示出来。
PART 03
逆向操作:增加“管道”,显著加速再生
既然“减少管道”会拖后腿,那么“增加管道”能否加速再生呢?研究团队进行了逆向实验。
研究人员以腺相关病毒(AAV)为载体,特异性地在肝细胞中过表达SLC25A51基因,相当于给肝细胞的线粒体安装了“增压泵”。结果显示,这些小鼠肝脏线粒体的NAD+水平大幅提升。
同样进行三分之二肝脏切除后,装上 “增压泵” 的小鼠展现出惊人的再生能力:肝脏再生速度显著加快,肝细胞增殖异常活跃,再生效果与全身补充 NAD + 前体不相上下。
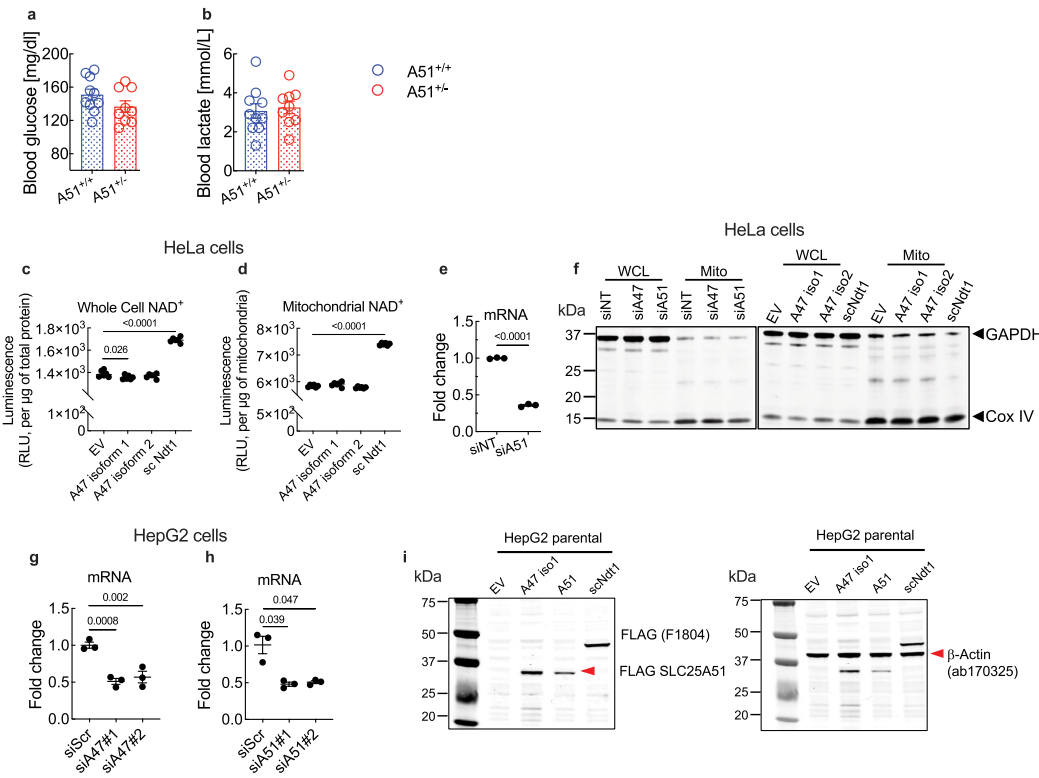
更关键的是,通过精密的细胞分馏技术检测发现,这种再生加速的益处,仅来自线粒体 NAD + 的提升,细胞质和细胞核的 NAD + 水平并未受影响。这一发现堪称“一锤定音”:提升肝细胞线粒体 NAD + 本身,就足以实现促进肝脏再生的效果,这也是 NAD + 前体发挥作用的核心原因。
PART 04
机制探秘:能量与原料的双重保障
为什么线粒体NAD+如此关键?研究人员从代谢组学和蛋白组学中找到了线索。肝脏再生是一个极其耗能的过程,需要大量合成新的细胞成分(如脂质、蛋白质)。当线粒体NAD+充足时,线粒体的呼吸功能,尤其是依赖于NAD+的复合物I活性和脂肪酸氧化能力更强,能为再生提供更充沛的ATP能量。
同时,SLC25A51过表达的肝脏表现出脂质代谢相关通路的上调。这意味着,线粒体NAD+不仅提供了“能量货币”(ATP),还可能通过影响细胞内的信号传导,促进了“建筑材料”(如脂肪酸)的合成,从而满足了再生过程中巨大的生物合成需求。
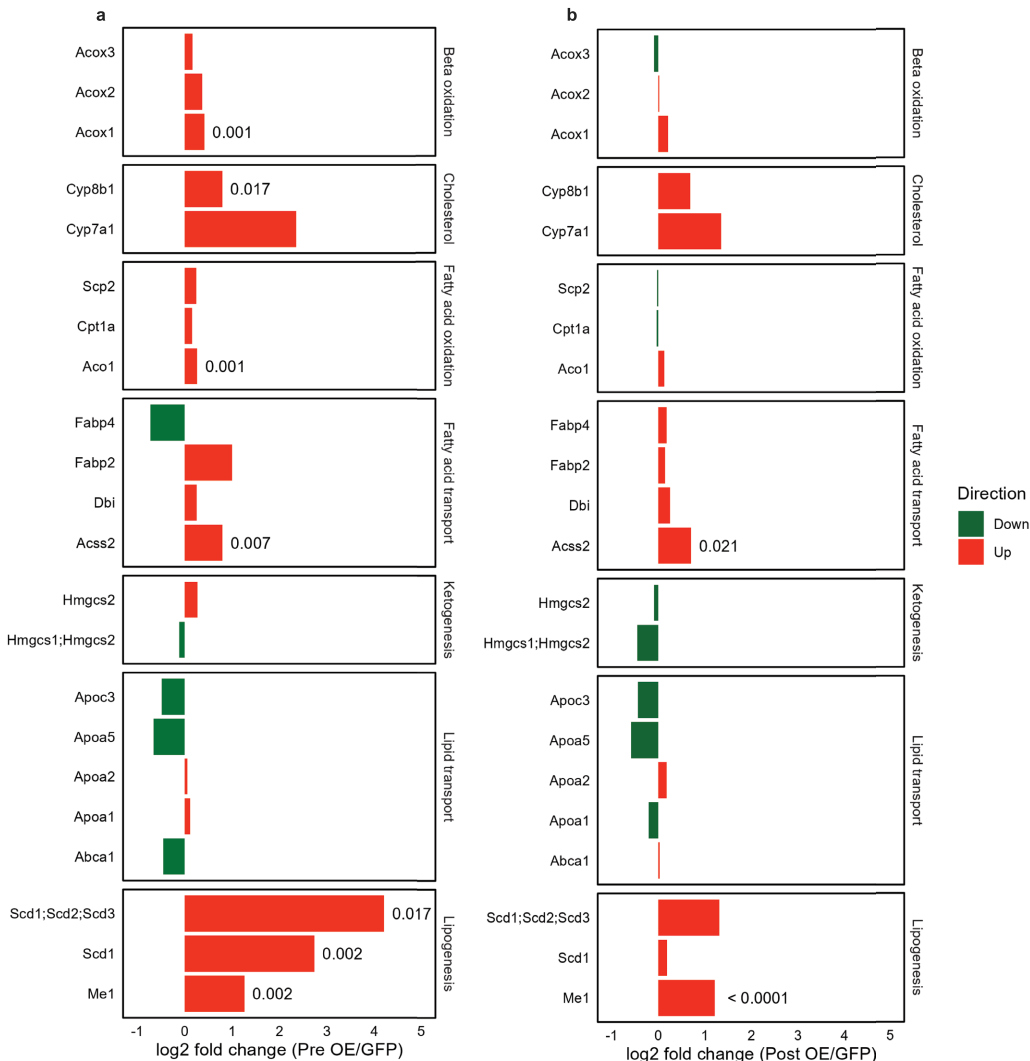
在再生压力下,对照组肝细胞线粒体内的多种代谢物被大量消耗;而在SLC25A51过表达的肝细胞中,这种消耗得到了缓解,代谢状态更稳定。这表明,高水平的线粒体NAD+像是一个“缓冲池”,帮助肝细胞更好地应对再生带来的巨大代谢压力。
PART 05
展望未来:从广谱补充到精准靶向,肝病治疗迎新思路
这项研究将NAD+生物学领域的认知,推向了一个全新的高度。它不仅明确了线粒体 NAD + 池是肝脏再生的核心治疗靶点,还解开了一个临床困惑:为何有时全身 NAD + 总水平变化不大,机体功能却出现问题?答案很可能是,关键部位的 NAD+“池子” 已经告急。这也提示未来,评估 NAD + 代谢状态,需要更精细地考察其亚细胞分布。
而其最大的价值,在于为临床转化和药物开发开辟了新思路。目前,通过口服NR、NMN等前体来补充NAD+,是一种“广谱”但略显“粗放”的策略。而这项研究则指明了一条 “精准”之路:
未来,科学家或许可以开发一种药物,像“钥匙”一样,特异性地激活肝脏里的SLC25A51“管道”,从而在需要的时候(如肝脏手术、药物性肝损伤后),精准地为肝细胞线粒体“快速充电”,极大地增强其再生修复能力。这既能达到甚至超越全身补充的效果,又能避免不必要的全身性影响。
当然,这项研究目前仅在雄性小鼠中完成,其结论是否适用于雌性,以及线粒体NAD+是否也是其他器官修复的关键,将是未来研究的重要方向。但无疑,我们已经拿到了打开肝脏再生奥秘之门的其中一把关键钥匙,对攻克肝脏疾病的未来,充满了更多期待。
参考文献:
Mukherjee S, Velázquez Aponte RA, Perry CE, Lee WD, Janssen KA, Niere M, Adzika GK, Lu MJ, Chan HR, Zou X, Chen B, Bye N, Xiao T, Yook JS, Salik O, Frederick DW, Gaspar RB, Doan KV, Davis JG, Rabinowitz JD, Wallace DC, Snyder NW, Kajimura S, Cambronne XA, Ziegler M, Baur JA. Hepatocyte mitochondrial NAD+ content is limiting for liver regeneration. Nat Metab. 2025 Dec;7(12):2424-2437.